Nach einem Verkehrsunfall soll ein Patient versorgt werden, der aus einem brennenden Auto gerettet wurde. Es findet sich ein Schädel-Hirn-Trauma, Mittelgesichtsverletzungen und Rußspuren nach Inhalationstrauma.
Zwei Sachen sind sicher:
1) dieser Patient muss intubiert werden und
2) das wird sicher nicht einfach.
Doch #KapnoFirst hilft! Denn hiermit kann:
- die effiziente Präoxygenierung sichergestellt werden
- eine Sauerstoffreserve für den Notfall geschaffen werden
- sofort eine Lagekontrolle erfolgen und ihr könnt (relativ) entspannt bleiben auch wenn die Sättigung nach der Intubation erstmal weiter fällt…

Einsatz überörtlich, Trauma nach VU.
Der Patient wurde bereits technisch durch die Feuerwehr gerettet und in den RTW verbracht.
Im RTW ist es sehr laut und unruhig, zu viele Leute auf zu engem Raum, der Patient wird entkleidet, jemand hält ihm eine Sauerstoffmaske vors Gesicht.
Im primary survey fallen auf
A: V.a. Mittelgesichtsverletzung, Rußspuren nach Inhalationstrauma, Schwellung, drohende Verlegung des Atemwegs aktuell durch Esmarch-Handgriff gelöst
B: V.a. stumpfes Thoraxtrauma beidseits VAG, SpO2 80% mit 12l Sauerstoff über Maske
C: Recap-Zeit deutlich verlängert
D: SHT mit GCS 6 (E1-V2-M3)
E: kalt, BZ normal
Es wird ein „10 für 10“ gemacht, alle sind sich einig, dass eine Intubation unumgänglich ist. Die Aufgaben für die geplante Stabilisierung und Narkoseeinleitung werden verteilt:
NA / RS RTW: Präoxygenierung
NFS RTW: Vorbereitung Tubus und Monitoring
NFS NEF: Vorbereitung Medikamente für die Narkose
Der Patient hat viel Sekret und Blut im Gesicht, die Maske ist nur leidlich dicht zu bekommen. Die SpO2 steigt mit assistierter Spontanatmung immerhin bis auf 94%.
Es fällt auf, dass die Atemanstrengungen des Patienten jetzt weniger werden. Als alles fertig ist wird die Narkose gespritzt, der Patient hört unmittelbar auf zu atmen. Trotz Präoxygenierung hat der Patient null Reserven die SpO2 fällt weiter jetzt 88%.
Die Maskenbeatmung ist deutlich erschwert, 82% - der Ton wird immer tiefer.
Videolaryngoskopisch ist die Sicht sehr schlecht, der Rachen ist voll mit Blut und Sekret. SpO2 78%.
Die Stimmritze (oder ist es doch der Ösophagus?) lässt sich nur erahnen, SpO2 75%, es kommt Unruhe im RTW auf.
Bougie dahin wo die Stimmritze sein müsste, SpO2 71%, Patient wird jetzt auch bradykard.
Tubus blocken, Filter drauf, Ambu-Beutel dran, erster Atemhub. SpO2 66%.
Der NFS hört den Magen mit dem Stethoskop ab - es blubbert. SpO2 60%.
Die Auskultation der Lunge ist nicht eindeutig. Das Signal der Sättigung bricht ab.
Und jetzt?
Rausziehen? When in doubt, pull it out habe ich mal gelernt.
Aber was wenn der Tubus doch richtig liegt?
Dann habe ich unwissentlich den schwierigen Atemweg gemeistert - um direkt danach mir selbst mehrere große Probleme zu schaffen und wieder von vorne anfangen zu müssen. Dann aber mit einem hypoxischen Traumapatienten im Periarrest.
Ich denke man kann sich ausmalen wie eine solche Situation ausgeht.
Ich glaube alle NotärztInnen und IntensivmedizinerInnen haben schon mal einen solchen Moment erlebt.
Schwierige Intubationsbedingungen, eine anästhesiefeindliche Umgebung und ein grenzkompensierter Patient - diese Konstellation ist in der Notfall- und Intensivmedizin recht häufig.
Selbst wenn der Tubus dann endotracheal platziert ist, kann es eine Weile dauern bis man an einem Anstieg der Sättigung über die Pulsoxymetrie erkennt, dass der Tubus richtig liegt.
Hier könnte das #KapnoFirst-Konzept helfen.
Für #KapnoFirst wird die Kapnographie so eingebaut, dass sie bereits bei der Präoxygenierung konnektiert und angezeigt wird.
Für das Setup empfiehlt sich der folgende Aufbau:
Gesichtsmaske > Gänsegurgel > HME-Filter > Kapnographie > Ambubeutel
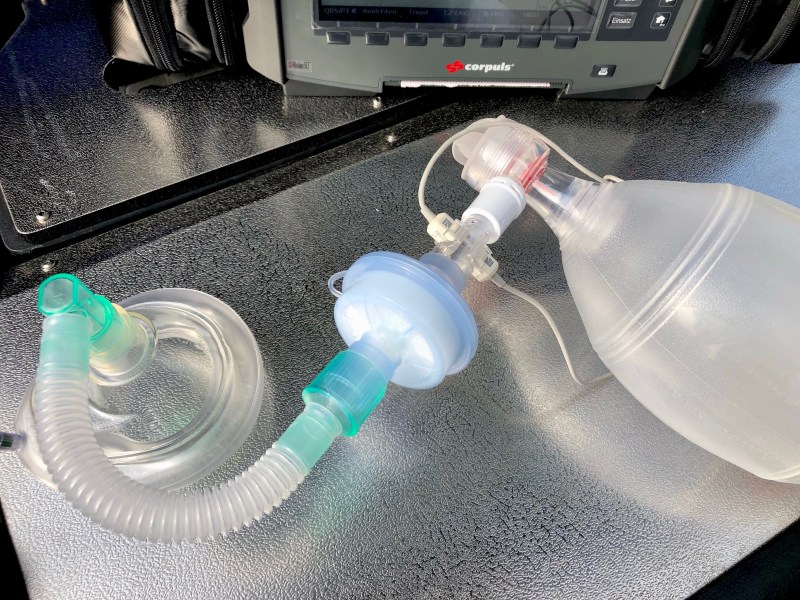
Bereits bei der Präoxygenierung leistet die Kapnographie wertvolle Unterstützung.
#KapnoFirst zur Präoxygenierung:
Wir drücken dem Patienten mit sanftem Druck eine Maske ins Gesicht über die er hochdosiert Sauerstoff bekommen soll - die Präoxygenierung.
Ein Abstand von nur 1 mm (!) bewirkt bereits einen Abfall der erreichbaren alveolären inspiratorischen Sauerstoffkonzentration (FiO2) auf 0,4–0,6 (Wilhelm et al., Praxis der Anästhesiologie, S. 271).
In der Klinik präoxygenieren wir für 3 Minuten oder mindestens 4-5 tiefe Atemzüge, idealerweise so lange bis die FeO2 ≥0,9 ist.
Wie überprüfe ich also ob meine Maske wirklich dicht sitzt und der Patient auch wirklich den Sauerstoff einatmet, den ich da vorhalte?
Auch hier hilft #KapnoFirst!
Eine plausible CO2-Kurve garantiert mir eine dicht sitzende Maske und eine suffiziente Präoxygenierung. Das ist die Reserve die Euch
und den Patienten retten kann!

In der Praxis wird die Kapnographie meist erst nach erfolgter - und hoffentlich erfolgreicher - endotrachealer Intubation angeschlossen.
Dann schaut man gebannt auf den Monitor und wartet auf ein Signal.
Und wartet.
Kein CO2-Signal.
Es macht sich Unruhe breit. Oh - falsches Display eingestellt!
Das Display steht noch auf „Standard“, (Abl. I,II, III und die Sättigung), es wird also schnell auf den „Intensiv“-Modus umgestellt.
Und wartet - und… wartet?
Kommt aber kein Signal. Oh, der Airway-Adapter war gar nicht konnektiert.
Währenddessen fällt die Sättigung oder vielleicht ist es sogar ein Szenario wie weiter oben beschrieben und irgendjemand verliert die Nerven und zieht den (unwissentlich eigentlich korrekt liegenden) Endotrachealtubus wieder heraus.
Habe ich die Kapnographie bereits zur Präoxygenierung angeschlossen, dann weiß ich, dass das System funktioniert. Bekomme ich dann nach einer ggf. unerwartet schwierigen Intubation nicht sofort ein CO2-Signal kann ich sofort reagieren. Bekomme ich hingegen sofort nach Intubation ein CO2-Signal, kann ich auch weiter fallende SpO2-Werte tolerieren weil ich weiß, dass sich diese dank der erfolgreichen endotrachealen Intubation rasch wieder erholen werden.
Die Kapnopgraphie ist:
1) das schnell verfügbare Hilfsmittel für den sofortigen, sicheren Nachweis einer erfolgreichen endotrachealen Intubation
2) eine Qualitätskontrolle für eine dicht sitzende Maske = eine suffiziente Präoxygenierung
3) häufig nicht richtig angeschlossen oder wird komplett vergessen oder das Display ist falsch eingestellt oder oder oder
4) in allen themenrelevanten Leitlinien obligat gefordert (u.a. S1-LL Prähospitales Atemwegsmanagement, Leitlinie “Prähospitale Notfallnarkose beim Erwachsenen“ und andere)
Die Rede ist von einer sogenannten 100%igen-Kapnographierate. Es gibt keinen Grund keine Kapnographie anzuschließen!
Im Rahmen einer komplexen Traumaversorgung, bei einem Kindernotfall oder auf der Intensivstation im septischen Schock - da gehen einem schnell die grünen Kügelchen aus und ich habe es mehrfach erlebt, dass ich PatientInnen übernehmen sollte, bei denen die Kapnographie im Eifer des Gefechts einfach vergessen wurde.
Die Berichte die es in die Tagespresse schaffen sind eher ein Eisbergphänomen, wenn man danach sucht, findet man zumindest genug weitere Beispiele wo die versäumte Kapnographie gravierende Konsequenzen nach sich zog.
Die notfallmäßige Intubation in der Präklinik oder auf der Intensivstation unterscheidet sich in wesentlichen Punkten von einer Intubation im Rahmen einer elektiven Operation:
| Präklinik | Intensivstation | OP | |
| Lagerungsbedingungen | schlecht | mäßig | sehr gut |
| Reserven des Patienten | keine/wenig | keine/wenig | sehr gut |
| personelle Reserven | wenig | eingeschränkt | optimal |
| Aspirationsrisiko | hoch | hoch | niedrig (Pat. nüchtern) |
| Routine in der Durchführung | sehr wenig | eher wenig |
sehr viel (Fachpflegekraft Anästhesie plus AnästhesistIn) |
| Teamzusammensetzung | immer neu | meist neu | oft bekannt |
Die Liste ist sicher nicht vollständig, aber es wird auch so ersichtlich, dass selbst ein hauptberuflich Narkosen durchführender Anästhesist im präklinischen oder intensivmedizinischen Setting besonderen Limitationen unterliegt. Umso mehr sollten KollegInnen die in der Atemwegssicherung und Narkoseführung eher ungeübt sind niederschwellig und frühzeitig Hilfsmittel wie die Kapnographie einsetzen - nicht erst bei einer Kindernarkose.
Und was machen wir mit KollegInnen die das nicht brauchen, weil sie das Narkotisieren noch vor der Kapnometrie-Zeit erlernt haben? Nun, die sollten vielleicht mal diesen Fall lesen - da ist eine 23-jährige ansonsten gesunde junge Frau im Rahmen einer Zahn-OP gestorben weil jemand selbstbewusst und selbstgefällig genug war auf diese zusätzliche Sicherheit zu verzichten.
Was passieren kann, wenn man nicht routinemäßig eine Kapnographie einsetzt ist eindrücklich im folgenden Artikel geschildert:
https://annemergmed.com/retrieve/pii/S0196064404014428
The Effectiveness of Out-of-Hospital Use of Continuous End-Tidal Carbon Dioxide Monitoring on the Rate of Unrecognized Misplaced Intubation Within a Regional Emergency Medical Services System
Salvatore Silvestri, MD et al.
Published:February 04, 2005DOI:https://doi.org/10.1016/j.annemergmed.2004.09.014
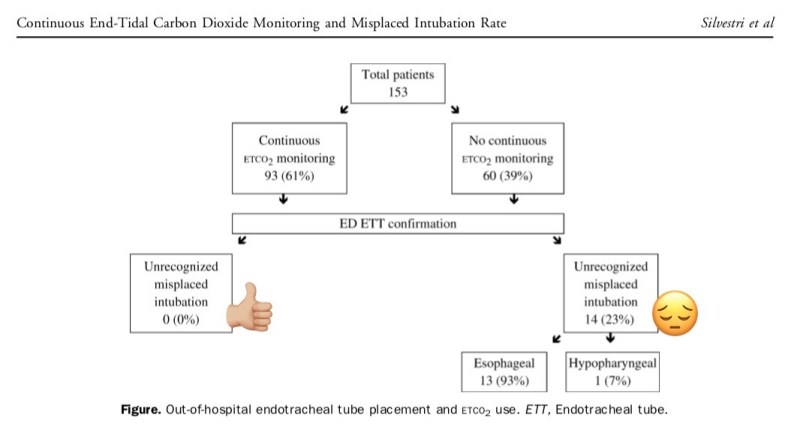
Von 153 präklinisch intubierten PatientInnen wurde in immerhin 39% der Fälle kein etCO2-Monitoring angebracht. Hiervon waren etwa ein Viertel falsch intubiert.
Oder in anderen Worten - es gibt wenig Dinge mit denen man Menschen so effektiv zu Schaden bringen kann wie mit dem Unterlassen einer Kapnographie.
Jule ist 7 Jahre alt, auf dem Nachhauseweg rennt sie fröhlich ihrem Freund hinterher. Zwischen zwei Autos bleibt sie stehen, wird am Kopf von dem Außenspiegel eines Fahrzeugs touchiert.
Ein RTW, ein NEF werden alarmiert. Obwohl Jule äußerlich nur leicht verletzt wirkt und auch voll orientiert ist, alarmiert die Notärztin vor Ort einen Hubschrauber wegen des Verdachts auf ein Schädel-Hirn-Trauma nach. Die Notärztin des RTH leitet schließlich eine Narkose ein und bemerkt die ösophageale Fehllage des Tubus nicht. Jules Zustand verschlechtert sich dramatisch und sie verstirbt noch während des Fluges.
Das ist leider keine erfundene Geschichte, sondern 1998 so passiert, nachzulesen in dem Buch „Du hättest Leben können“. Das Buch enthält viele gute Gedanken zu dem Mythos ärztlicher Unfehlbarkeit, unserer Fehlerkultur und dem Streben nach Gerechtigkeit.
Ich denke der Stellenwert der Kapnographie ist klar geworden.
Wenn wir aber ohnehin die Kapnographie einsetzen müssen, warum sollte ich sie dann nicht schon direkt zur Präoxygenierung nutzen?
Nur so kann ich entspannt abwarten, wenn die Sättigung nach der Intubation fallen sollte, aber das CO2-Signal schon da ist.
Wenn ihr wissen wollt, wie ihr noch ein Level weiter kommen wollt und vielleicht sogar ganz einen Sättigungsabfall verhindern könnt, dann empfehle ich Euch dringend den Artikel zur delayed sequence intubation (DSI) zu lesen bzw. zur Bedeutung der Reihenfolge der applizierten Medikamente in dem Artikel Rocketamin vs. Keturonium.
Ich würde mich freuen, wenn ihr das Konzept #KapnoFirst mal bei Euch vorstellt oder über eine Checkliste direkt in Eure präklinische oder intensivmedizinische Tätigkeit einbaut.
Für Rückfragen schreibt mir am liebsten direkt eine DM bei Twitter.
Vielen Dank!
Für alle die keine Zeit haben, #KapnoFirst meint:
Die Kapnographie muss ohnehin immer angeschlossen werden.
Bei Indikation zur Notfallintubation daher immer bereits gemeinsam mit dem Beatmungsbeutel und der Gesichtsmaske die Kapnographie direkt mit konnektieren und schon für die Präoxygenierung nutzen. Nur so ist eine suffiziente Präoxygenierung garantiert und auch nach einer schwierigen oder unsicheren Intubation eine direkte Verifzierung der Tubuslage ohne Zeitverzug möglich.
AUTOR:
Daniel Dreyer (@doc_emed), Facharzt für Anästhesiologie, Spezielle Intensivmedizin, Notfallmedizin. Nach vielen Jahren mit Intensivtransporten, Luftrettung und Blut, Schweiß und Tränen im Schockraum schlägt mein Sinusrhythmus jetzt in einem Haus am See.
Wie immer gilt: Der Einzelfall entscheidet. Der Artikel erhebt keinen Anspruch auf Vollständigkeit oder Richtigkeit und die genannten Empfehlungen sind ohne Gewähr. Die Verantwortung liegt bei den Behandelnden. Der Text stellt die Position des Autors dar und nicht unbedingt die etablierte Meinung und/oder Meinung von dasFOAM.




Hallo, vielen Dank für den eindrucksvollen Artikel! Ich würde die Kapnometrie immer so patienten-nah wie möglich platzieren, damit CO2 auch bei geringem Zugvolumen rasch und zuverlässig detektiert werden kann. Das gezeigte Foto zeigt jedoch eine “Gänsegurgel” zwischen Maske und CO2-Küvette gesteckt, die den Totraum gefährlich verlängert. Dies behindert nicht nur die CO2-Detektion, sondern auch das Abventilieren von CO2. Ich würde die Gänsegurgel prinzipiell weglassen, und den Filter mitsamt CO2-Meßküvette direkt an die Maske anstecken.
Hallo Roger,
vielen Dank für die Ergänzung!
Es war nicht für alles Platz in dem Text. Sowohl die Tubusverlängerung (“Gänsegurgel”) als auch der Ort des CO2-Adapters sind bewusst gewählt.
Warum überhaupt eine Tubusverlängerung?
Man kann das Setup auch ohne Tubusverlängerung zusammen stecken, dann wird es sehr starr. Maske, darauf den HME-Filter, darauf den CO2-Adapter, dann der Beutel mit Einmembranventil und 90°-Adapter… das ist viel Gewicht was direkt im Gesicht des Patienten hängt und eine Maskenbeatmung erschwert.
Außerdem kann so direkt nach Intubation die Maske abgehangen und direkt an den ETT angeschlossen werden.
Warum den CO2-Adapter nicht direkt an die Maske sondern dahinter?
Zu ihrem Einwand der verspäteten/verzögerten Messung - das ist eine theoretische Überlegung. Probieren Sie es mal aus - in der Praxis ist bezüglich der Anschlagszeit kein Unterschied feststellbar. Unter Laborbedignungen wird man sicher einen Unterschied messen können, in der Praxis ist dieser nicht feststellbar.
Es gibt aber einen guten Grund den CO2-Adapter HINTER den HME-Filter zu positionieren. Wenn man den CO2-Adapter wie vorgeschlagen direkt an den Tubus anschließt kann dieser durch Sekret (Aspiration, Lungenödem, Blut etc.) sehr schnell unbrauchbar werden. Dann hat man nichts gewonnnen, dann geht nämlich erstmal die Suche nach einem neuen Adapter los.
Alternativ könnte man höchstens die Reihenfolge Maske > HME-Filter > CO2-Adapter > (Gänsegurgel) > AmbuBeutel wählen. Dann hat man aber wieder einen recht hohen “Tannenbaum” im Gesicht des Patienten, das finde ich vom Handling eher unpraktisch - ohne nennenswerte Vorteile.
So oder so - hauptsache die Kapnografie ist bereits bei der Präoxygenierung am Start 😉
Viele Grüße!
Daniel
Ich finde die Antwort sehr gut und nachvollziehbar. Kennst du oder jemand sonst hierzu eine valide Quelle oder geht es euch so wie mir, dass der “Tannenbaum” oder wie ich sage “Trompete” vier Zug am Tubus bzw. an der Maske mit sich bringt.