Eine Zusammenarbeit von Dr. Smiths EKG-Blog und EMCrit - übersetzt von dasFOAM in Zusammenarbeit mit Pendell Meyers
Originalautoren: Pendell Meyers, MD, Scott Weingart, MD, FCCM, Stephen Smith, MD, eine gemeinsame Bearbeitung der Übersetzung von Wilma Bergström, Aurelia Hübner, Felix Lorang, Lisa Rossbach, Joachim Unger und Justus Wolff.
Das aktuelle leitliniengetreue Konzept zur Behandlung des akuten Myokardinfarkts (“STEMI vs. NSTEMI”) ist mangelhaft (inhaltlich falsch) und hat während der letzten 25 Jahre bedeutende wissenschaftliche Fortschritte in der Therapie desselben verhindert. Dr. Stephen Smith bekräftigt dies in seiner Vortragsreihe schon seit einiger Zeit - und es lohnt sich, diese Erkenntnis weiter zu verbreiten.
Es ist schwierig zu entscheiden, welche Patienten eine schnelle Reperfusionstherapie (PTCA) benötigen und unsere derzeitigen STEMI-Kriterien sind dazu schlicht nicht geeignet. Patienten, die im Akutfall von einer Intervention profitieren, sind solche mit akuter und vollständiger Verlegung von Koronararterien (Okklusiver Myokardinfarkt - OMI) oder solche mit einer nahezu kompletten Okklusion und darunter ungenügender Durchblutung, bei denen ohne sofortige Reperfusionstherapie die unmittelbare Gefahr einer Nekrose bestünde. Soviel zur physiologischen Grundlage der Patientengruppe, die wir als “STEMI”-Patienten bezeichnen sollen. Leider beschränkt der Begriff “STEMI” unser Denken dahingehend, dass dieses Krankheitsbild zuverlässig nur durch die “STEMI-Kriterien” und damit anhand des ST-Segments im EKG diagnostiziert werden könnte. In der Realität haben STEMI-Kriterien und auch die Herzinfarkt-Diagnostik mit dem gegenwärtigen STEMI-Konzept eine inakzeptable Genauigkeit. Es werden regelmäßig mindestens 25-30% der okklusiven Myokardinfarkte in als “NSTEMI” abgestempelten Fällen übersehen und gleichzeitig eine etwa identisch hohe Rate an unnötigen, weil falsch positiven, Herzkatheterlabor-Aktivierungen verursacht.
Das STEMI/NSTEMI-Schema war damals im Jahr 2000, als die Denkweise Q-Wellen- vs. Nicht-Q-Wellen-Myokardinfarkt formell abgelöst wurde, noch die beste unter den neuen Ideen. Dieser Paradigmenwechsel wurde durch die Reperfusionsära eingeläutet, in der mehrere große Studien die Wirksamkeit einer schnellen Reperfusionstherapie belegten. Dank Dr. Smith und anderen haben wir seitdem eine Menge Neues über die tiefergehende Interpretation von EKGs gelernt. Es stellte sich unweigerlich heraus, dass die ST-Hebung allein im EKG wohl doch nicht mehr das beste Anzeichen für die Obstruktion eines Koronargefäßes ist und damit für sich allein zur Indikationsstellung einer Reperfusionstherapie nicht ausreicht.
Für all diejenigen mit viel Erfahrung und Patientenkontakten, die EKGs mit anschließenden Angiogrammen bei akutem Myokardinfarkt verglichen haben, ist es offensichtlich, warum die STEMI-Kriterien routinemäßig in beide Richtungen versagen. In erster Linie ist der akute Koronarverschluss ein komplexer und dynamischer Prozess, der nicht immer EKG-Veränderungen hervorruft. Selbst wenn sich EKG-Veränderungen manifestieren, ist es ein komplizierter und sehr zeitabhängiger Verlauf, der besonders empfindlich auf (zufällige) Reperfusion und Reokklusion reagiert. Die frühen Stadien des Myokardinfarktes (wenn der Nutzen einer Intervention am größten ist) zeigen regelhaft keine ST-Hebungen. Selbst wenn man gerade Glück hat (oder klug genug ist) und ein EKG in der Phase von ST-Streckenveränderungen schreibt, ist die ST-Hebung immer proportional zur Größe des QRS-Komplexes. Und der kann im Standard-12-Kanal EKG bei einigen Myokardgebieten (z.B. basolateral) mitunter sehr klein sein. Darüber hinaus produzieren nicht alle Herzinfarkte ST-Hebungen, manche führen nur zu Veränderungen im QRS-Komplex, der T-Welle, oder eben gar keinen pathologischen EKG-Befunden. Dies kann auf eine Vielzahl von Ursachen zurückzuführen sein: Den Zeitpunkt der Aufzeichnung (einschließlich während einer kurzen Periode spontaner Reperfusion), Infarkt in einem nicht gut auf dem EKG ‘sichtbaren’ bzw. sehr kleinen Myokardgebiet oder niedrige QRS Amplitude. Währenddessen zeigen sich bei vielen Menschen ohne ACS ST-Hebungen im EKG als normale Variante oder verursacht durch eine abnorme Depolarisation (Linksventrikuläre Hypertrophie als häufiges Beispiel), die dann fälschlicherweise STEMI-Kriterien erfüllen.
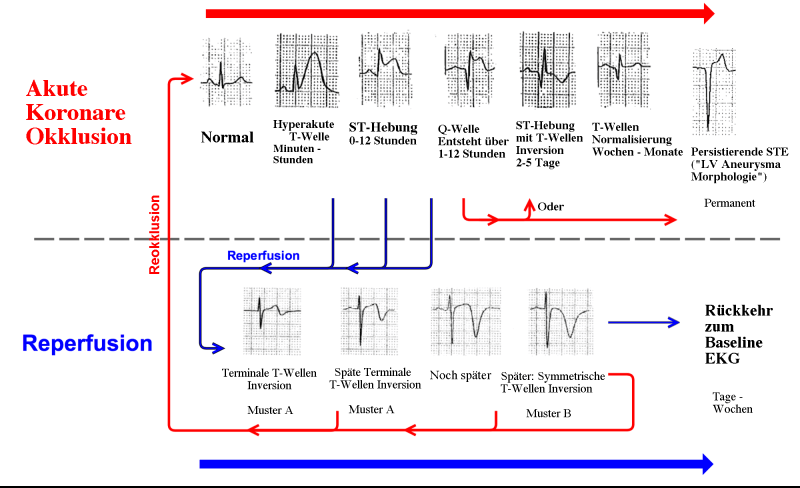
Zu lange wurde jetzt schon versucht, den bekannten, einprägsamen und allseits geliebten Begriff “STEMI” beizubehalten und durch die Einführung von zusätzlichen Bezeichnungen wie “STEMI Äquivalent” das offensichtliche Problem anzugehen, obwohl in Wirklichkeit der Name selbst Teil des Dilemmas ist. Der Begriff “STEMI” schränkt unser Denken dahingehend ein, dass nur die ST-Segmente wichtig wären, immer zuverlässig sind und nicht von den vorausgehenden QRS-Komplexen abhängen, und dass schließlich ST-Hebungen auf dem EKG die einzig notwendigen Kriterien sind, um die Indikation zur Behandlung zu stellen. Wenn wir größere Fortschritte bei der Behandlung akuter Myokardinfarkte erzielen wollen, sind wir gezwungen uns weiterzuentwickeln, und zwar weg von den derzeit verwendeten Begrifflichkeiten.
“Hat der Patient einen STEMI?” muss unausweichlich durch etwas ersetzt werden, das uns an die eigentlich wichtige Frage erinnert: “Hat der Patient einen akuten Verschluss der Koronararterien und würde er deshalb von einer sofortigen Intervention profitieren?”
Um das zu erreichen, schlagen wir die folgenden Begriffe als Alternative vor:
OMI = Okklusiver Myokardinfarkt
NOMI = Nichtokklusiver Myokardinfarkt
Teil I: (Die Geschichte vom STEMI und der Reperfusion)
In der Reperfusion-Ära wurde versucht, einige wichtige Fragen zu beantworten:
- Funktioniert die Reperfusionstherapie?
- Wie sollten wir prospektiv und nichtinvasiv herausfinden, wer eine Notfall-Reperfusion erhält?
Die gute Nachricht ist, dass wir eine dieser beiden Fragen abschließend beantworten konnten: Die Reperfusionstherapie funktioniert. Thrombolytika erwiesen sich bei fast 60.000 Patienten als lebensrettend, die in der Reperfusions-Ära Thrombolytika randomisiert gegenüber Placebo erhielten, und zwar in einem der stärksten Beweise in der Geschichte der Medizin. Vor dieser Entdeckung war das vorher existierende Paradigma einfach “Q-Wellen oder Nicht-Q-Wellen-Myokardinfarkt”. Die Kliniker hatten in der akuten Phase des Myokardinfarktes weniger effektive Therapien zur Verfügung und mussten einfach die Patienten beobachten, während diese ihren transmuralen Infarkt ausbildeten. Später, falls der Patient noch am Leben war, würden die Patienten danach klassifiziert werden, je nachdem, ob ihr EKG die für den transmuralen Infarkt typischen Q-Wellen entwickelte.
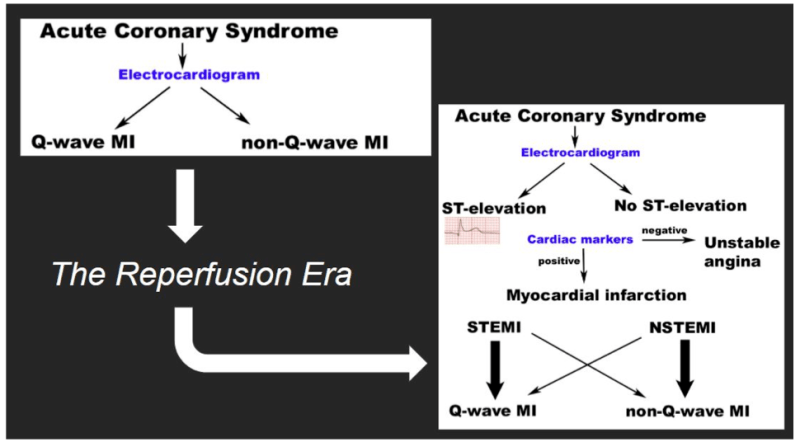
Aber wer profitiert denn eigentlich von potenziell gefährlichen Interventionen, um eine Koronararterie wieder zu öffnen? Natürlich Patienten mit akutem Verschluss der Koronararterien. Es gibt keine andere Theorie oder Evidenz, die einen möglichen Nutzen der Reperfusionstherapie nahe legt, außer um eine akute Okklusion (oder Fast-Okklusion mit unzureichender Perfusion durch Kollateralgefäße) wieder zu beheben. Wenn Patienten nicht Teil dieser Kohorten sind, so können sie nicht von der Intervention profitieren, aber werden trotzdem allen Nebenwirkungen ausgesetzt.
Die schlimmsten Komplikationen der Koronarangiographie sind Koronardissektionen und -perforationen, die grundsätzlich durch die eigentliche Koronarintervention und nicht den diagnostischen Teil der Angiographie bedingt sind. Dennoch werden alle Patienten, die sich einer notfallmäßigen Koronarangiographie unterziehen (auch die falsch-positiven, die keine Intervention erhalten), mit Folgen konfrontiert: Verfrühtes Ausschließen einer Diagnose (mit möglichen Schäden abhängend von der übersehenen bzw. dann erst verzögert gestellten Diagnose), Blutungskomplikationen durch die arterielle Punktion wie Leistenschmerzen oder retroperitoneale Hämatome, verschlimmert durch Medikation mit mehreren Thrombozytenaggregationshemmern und Antikoagulantien, kontrastmittelassoziierte Nephropathie, Strahlenbelastung und große Kosten- wie Ressourcenmobilisierung.
Im schlimmsten Fall gibt es einige Patienten mit Zufallsbefunden in Form einer eigentlich chronischen KHK, die nur aufgrund eines imponierenden nicht-ischämischen EKGs (z.B. ST-Hebungen als normale Varianten wie oben aufgeführt, die zufällig die STEMI-Kriterien erfüllen) schließlich auf dem Tisch des Herzkatheter-Labors landen. Normalerweise hätten diese Patienten gar keine Angiographie bekommen, da sie im Verlauf mehrere negative Troponine gefolgt von einem negativen Stresstest gehabt oder gleich aus dem Krankenhaus entlassen worden wären. Wenn diese dann im Herzkatheter landen und der Kardiologe die 70%-ige chronische atherosklerotische Koronarstenose vorfindet, wird diese oft behandelt, obwohl sie weder akut ist noch die Ursache der Beschwerden und EKG-Befunde erklärt. Diese Patienten erhalten also den gesamten Satz an oben genannten Risiken, einschließlich Dissektionen und Perforationen, ohne Aussicht auf einen Nutzen.
Es scheint fast schmerzhaft offensichtlich, aber wir müssen es immer wieder wiederholen um uns vor Augen zu führen, wie weit wir vom Weg abgekommen sind: Patienten mit Okklusions-MI (oder Beinahe-Okklusion mit unzureichenden Kollateralgefäßen) sind die einzigen, die von einer notfallmäßigen Reperfusionstherapie profitieren. Unabhängig davon, was das EKG zeigt. Patienten mit akutem Myokardinfarkt ohne Okklusion (NOMI) brauchen keine notfallmäßige Angiographie, auch wenn notfallmäßige Reperfusion im Vergleich mit dringender Angiographie wahrscheinlich keinen Schaden bei dieser Subgruppe anrichtet. Alle Andere sind dem Risiko von Schaden ohne Nutzen ausgesetzt und brauchen keinen notfallmäßigen Herzkatheter.
Wie wurde also in den Studien, die die Wirksamkeit der Reperfusionstherapie im Vergleich zu Placebo bewerten sollten, bestimmt, wer ein ACS hat?
Gar nicht. Alle Placebo kontrollierten Studien fanden in der Ära der Thrombolyse statt! Angiographie wurde in diesen Studien vor der Therapie nicht angewendet, selbst dann nicht, wenn sie verfügbar war. Anstatt herauszufinden, wer ein ACS hatte (eine Diagnose, die man demnach gar nicht stellen konnten), randomisierten sie Patienten mit sehr hohem Risiko mit akuten Schmerzen in der Brust, die meisten mit relevanten, aber undefinierten EKG-Befunden in eine Placebo- und eine Thrombolysegruppe und beobachteten die Mortalität ohne zu wissen welche Patienten überhaupt ein ACS hatten.
Bevor irgendeine Subgruppenanalyse durchgeführt wurde, erhielt die gesamte Population von 56.600 Patienten im Durchschnitt einen signifikanten Mortalitätsvorteil (NNT = 56) durch die Thrombolytika im Vergleich zu Placebo. Vier der neun randomisiert kontrollierten Studien dieser Metaanalyse setzten zur Teilnahme keinerlei EKG Veränderungen voraus und ein Drittel der Patienten hatte keine ST-Strecken Erhöhung. Trotz dieser Tatsache rettete die Lyse Leben in der Gesamtpopulation, und zwar noch bevor Untergruppenanalysen bezüglich der EKG-Ausprägungen durchgeführt wurden. Dies kann nur bedeuten, dass die Kliniker eine Anfangspopulation mit einer ausreichend hohen Prävalenz von koronaren Verschlüssen ausgewählt haben, sodass der Vorteil der Lyse bei ACS-Patienten groß genug war, um den Schaden bei den Patienten ohne ACS auszugleichen.
Angesichts der enormen Stichprobengröße war der nächste logische Schritt eine Untergruppenanalyse, um bestimmte Gruppen zu identifizieren, die höhere oder niedrigere Sterblichkeitsvorteile (oder Schäden) durch die Interventionen hatten. Sie haben wichtige Zeitvorteile bei der Intervention in Verbindung mit dem Beginn der Symptome herausgearbeitet, die nicht Teil dieser Abhandlung sind, aber durch das Sprichwort „time is muscle“ verewigt wurden.
Als nächstes verglichen sie die Auswirkungen von Thrombolytika bei allen Patienten mit der Auswirkung nur in der Untergruppe der Patienten mit bestimmten EKG Veränderungen. Die Untergruppen bestanden aus “ST-Senkung”, “ST-Erhöhung” und “normal“. Leider haben nur vier der randomisiert kontrollierten Studien (RCTs) ihre Version von “ST-Hebung” definiert und diese vier hatten unterschiedliche Cut-Offs und verschiedene Methoden der Vermessung (meistens nicht einmal spezifiziert) verwendet.
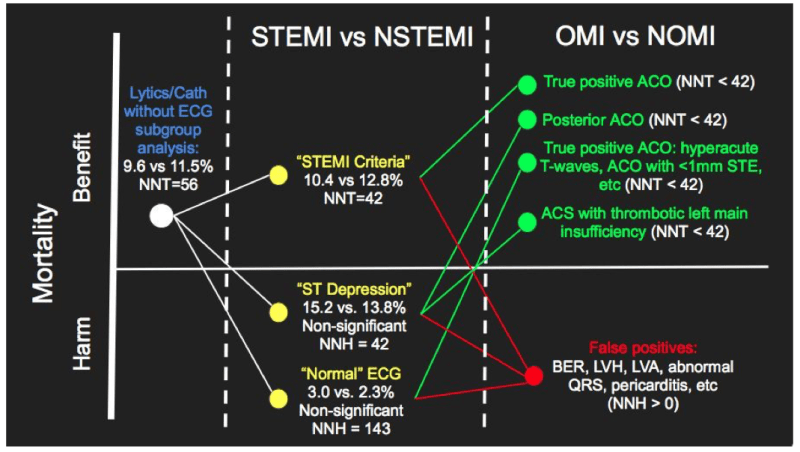
Im Vergleich mit der undifferenzierten Lyse für alle Patienten unabhängig von deren EKG-Befunden führte die Berücksichtigung einer undefinierten ST-Strecken-Hebung zu einer Reduktion der NNT für die Kurzzeitmortalität von 56 auf 43. Entgegengesetzt dazu zeigten die Untergruppen der “ST-Senkungen” und “normalen” EKGs einen nicht signifikanten Mortalitätsschaden (mit anderen Worten, keinen Nutzen). Es wurde keine weitere Untergruppenanalyse durchgeführt, um besser zu definieren, welche Patienten einen Sterblichkeitsvorteil versus einen Schaden hatten. “Normal” und “ST Senkung” wurden ebenfalls nicht weiter definiert.
Wie wir uns erinnern, kann notfallmäßige Reperfusion nur bei einer akuten Okklusion oder Beinahe-Okklusion einen Nutzen haben. Das führt zu der Schlussfolgerung, dass die Untergruppe der Patienten mit ST-Hebung einen höheren Anteil an Patienten mit ACS gehabt haben muss als die Gruppen ohne STE. Das macht intuitiv Sinn: Wenn eine Gruppe alle offensichtlichen “STEMIs” hat und die andere Gruppe nicht, wird die Gruppe mit den offensichtlichen “STEMIs” wahrscheinlich den höheren Anteil an ACS und daher den höchsten Mortalitätsvorteil durch Lyse haben. Aber aus Ihrer Erfahrung wissen sie wahrscheinlich, dass es auch viele falsch Positive in der STE-Untergruppe gibt (Patienten mit STE, aber ohne ACS), und viele falsch Negative in der Nicht-STE-Gruppe (Patienten ohne STE, aber mit ACS), welche alle eine größeres Mortalitätsrisiko haben indem sie in der falschen Gruppe sind.
In der STE-Gruppe der FTT-Meta-Analyse erkennen Sie zum Beispiel, dass es Patienten mit Normvarianten der ST Hebung („Frühe Repolarisation“), linksventrikuläre Hypertrophie, LV-Aneurysma, Takotsubokardiomyopathie, Perikarditis, diskordante ST-Hebungen auf Grund von abnormalen QRS-Komplexen etc. geben muss. Jeder dieser Patienten in der Lyse-Gruppe hatte ein Risiko von 1-2% durch die Gabe von Lyse innerhalb der ersten 24h zu sterben, ohne die grundlegende Chance auf irgendeinen Nutzen, da sie ja keinen akuten Verschluss hatten.
Umgekehrt gab es in den “normalen” EKG- und ST-Senkungs-Untergruppen sicherlich ACS-Patienten mit
- hyperakuten T-Wellen,
- subtilen ST-Hebungen, die geringer waren als der undefinierte Cutoff,
- posterioren Infarkten, die nur als präkordiale ST-Senkungen zu sehen waren,
- und diffuse subendokardiale Ischämien mit ST-Senkungen in vielen Ableitungen auf Grund der Größe des Thrombus etc..
Jedem dieser Patienten in der Placebogruppe ging ein Behandlungsvorteil verloren, da keine Lyse gegeben wurde.
Auch wenn durch ST-Hebung ein ACS besser diagnostiziert wird als durch gar keine EKG-Interpretation, sollte es klar sein, dass es Optionen für Verbesserungen gibt. Dies war in der FTT-Meta-Analyse leider nicht möglich, weil sie EKG-Befunde nicht mit durch Angiographie bewiesenen Okklusionen vergleichen konnten. Es ist lobenswert, dass die Kollegen dem logischen Ansatz - nämlich dass ein EKG ein nützliches Werkzeug ist um einen akuten Koronarverschluss zu finden - gefolgt sind, da es damit schnell, einfach, nichtinvasiv und überall identifiziert werden kann…
Aber rufen wir uns ins Gedächtnis, dass die FTT Meta-Analyse 1994 publiziert wurde und die meisten Studien, auf denen sie basierte, in den 1980er Jahren durchgeführt wurden. Seitdem haben wir unser medizinisches Management und unsere Techniken der mechanischen Reperfusion erheblich verbessert. Vermutlich schauen Sie jetzt mit Begeisterung auf die Literatur nach 1994 in der Annahme, dass nach 25 Jahren Erfahrung in routinemäßiger Katheterisierung es inzwischen sicherlich großflächige Forschung gibt, die uns hilft EKG-Veränderungen und Koronarverschluss noch besser in Verbindung zu bringen als es 1994 möglich war.
Unerklärlicherweise liegen Sie mit dieser Annahme fast vollständig falsch. Obwohl sich die Interventionen selbst stetig verbessert haben, gab es im offiziellen Vorgehen zur Identifizierung von Patienten, die von einer notfallmäßigen Intervention profitieren, seit 1994 kaum nennenswerte Fortschritte. Statt einer Liste aus relevanten Publikationen über 25 Jahre, die systematisch unsere EKG Kriterien dadurch verbessern, dass EKG-Veränderungen mit Angiographie-Befunden korreliert werden, findet man 25 Jahre an methodisch nicht anwendbaren Studien und –Richtlinien, die sich über STE-Millimeter-Kriterien streiten. Und das ohne irgendeine rationale Überlegung darüber, was wir vorhersagen können, wenn der Cutoff in V3 von 1,5 auf 2,0 mm und wieder zurück geändert wird.
Anhand der relevanten und in den Leitlinien zitierten Publikationen seit 1994 werden wir das im nächsten Teil auch nachweisen.



6 Kommentare