Wir wollten hier den Begriff NSTEMI zwar nicht mehr verwenden (my bad, das OMI-Manifesto findet ihr genau deswegen hier), doch ließ sich das Akronym beim Überblick über folgende, kürzlich erschienene Studie mal wieder nicht vermeiden:
Association of Parenteral Anticoagulation Therapy With Outcomes in Chinese Patients Undergoing Percutaneous Coronary Intervention for Non–ST-Segment Elevation Acute Coronary Syndrome
Die ERC-Guidelines empfehlen die parenterale Gabe von Antithrombinen in Kombination mit Acetylsalicylsäure (ASS) als wichtigen therapeutischen Zusatz zu Lysebehandlung oder PCI bei PatientInnen mit STEMI oder instabiler Angina Pectoris. Prä- oder erst intrahospital zur Auswahl stehen unfraktioniertes Heparin (abgekürzt UFH) als indirekter Thrombin-Inhibitor, Fondaparinux (niedermolekulares Heparin) als selektiver Faktor Xa-Antagonist oder Bivalirudin als direkter Thrombininhibitor. Bei Letzteren erübrigt sich ein Monitoring partieller Thromboplastinzeit, außerdem zeigt er ein geringeres Risiko heparin-induzierter Thrombozytopenien. Auch im Rahmen eines NSTEMI wird die parenterale Antikoagulation zum Zeitpunkt der Diagnosestellung empfohlen, was mit einer deutlichen Reduktion schwerwiegender kardialer Ereignisse (MACE) begründet wird. Während der Durchführung einer PCI wird die Heparinisierung generell empfohlen. Auch die AHA-Guidelines von 2014 empfehlen unfraktioniertes Heparin in einer loading-dose von 60 IE/kgKG mit anschließender kontinuierlicher Gabe von 12 IE/kgKG/h bis 48h nach Aufnahme oder erfolgter PCI. Die zugrundeliegenden Studien wurden primär an PatientInnen mit instabiler AP durchgeführt und stammen noch aus einer Zeit vor flächendeckend verfügbarer “früher” Revaskularisationstherapie und dualer Thrombozytenaggregationshemmung (TAH). Die Rolle von Heparin in der Akuttherapie und ein fragwürdiges Risiko-Nutzen-Verhältnis wird schon seit längerem diskutiert, einen weiteren Überblick über verschiedene randomisiert-kontrollierte Studien zusätzlich zu unserer Besprechung gibt es bei First10EM.
Nun aber zur Studie:
Design:
- Retrospektive Kohortenstudie
- Überprüfung einer Verbindung zwischen parenteraler Antikoagulation und klinischem Outcome bei PCI-PatientInnen mit NSTEMI in 5 chinesischen Zentren
- Vergleich zwischen:
Parenterale Antikoagulation mit unfraktioniertem Heparin vor PCI (PAK)
vs.
Parenterale Antikoagulation mit Fondaparinux / niedermolekularem Heparin lediglich während PCI (nPAK)
Endpunkte:
Primär:
- Generelle inhospitale Mortalität
- Schwere, inhospitale Blutung
Sekundär:
- Jegliche Blutung
- Myokardinfarkt
- Kombinierter Endpunkt aus Tod, Myokardinfarkt oder schwerer Blutung
- Kombinierter Endpunkt aus Tod oder schwerer Blutung während Follow-Up
Inklusionskriterien:
- Erwachsene PatientInnen mit NSTEMI, die mit parenteraler Antikoagulation vor oder während PCI behandelt wurden
Exklusionskriterien:
- Parenterale Antikoagulation nach PCI
- Schwangerschaft
- Kardiogener Schock mit IABP
- andere Indikation für Antikoagulation
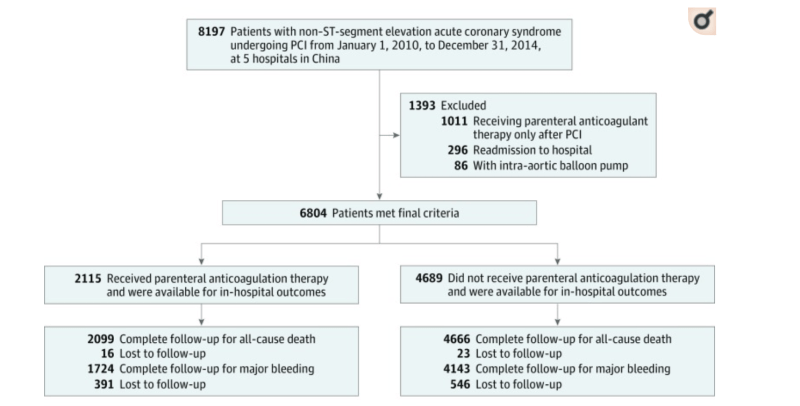
Insgesamt entsprachen 6804 PatientInnen den finalen Kriterien – davon erlitten 57,3 % einen NSTEMI und 42,7 % wurden mit instabiler Angina Pectoris abschließend diagnostiziert. 2115 dieser Patienten erhielten parenterale Antikoagulation, 4689 erhielten keine parenterale Antikoagulation.
Resultat:
Inhospitale Mortalität:
- mit Antikoagulation: 0,3 %
- ohne Antikoagulation: 0,1 %
- aOR 1,27; 95 % CI 0.38 – 4.27; p = 0.70
Myokardinfarkt:
- mit Antikoagulation: 0,3 %
- ohne Antikoagulation: 0,3 %
- aOR 0.77; 95 % CI 1.24 – 3.03; p = 0.004
Schwere Blutung inhospital:
- mit Antikoagulation: 2,5 %
- ohne Antikoagulation: 1,0 %
- aOR 1.94; 95 % CI 1.24 – 3,03; p = 0.004
Kombinierter Endpunkt aus Tod, Myokardinfarkt oder schwerer Blutung
- mit Antikoagulation: 3,0 %
- ohne Antikoagulation: 1,4 %
- aOR 1.54; 95 % CI 1.04 – 2,30; p = 0.03
Langzeit-Follow-Up (gemittelt 2,96 Jahre)
- Tod: kein Unterschied
- Schwere Blutung: höheres Risiko in Gruppe mit parenteraler Antikoagulation (zumeist in den ersten 30 Tagen)
Fazit der Autoren:
“In the patients undergoing percutaneous coronary intervention for non-ST-segment elevation acute coronary syndrome, parenteral anticoagulation therapy was not associated with a lower risk of all-cause death or myocardial infarction but was significantly associated with a higher risk of major bleeding. These findings raise important safety questions about the current practice of routine parenteral anticoagulation therapy while we await randomized trials of this practice.”
Als erste Studie, die den Zusammenhang zwischen parenteraler Antikoagulation und klinischem Outcome adressiert, finden sich trotz retrospektivem Studiendesign einige Stärken:
- Alle klinischen Ereignisse wurden von einem zu Behandlungsdetails verblindeten Kommittee einzeln bewertet
- Jegliche Daten bezüglich antithrombotischer Medikation wurden gesammelt (Dauer der Anwendung, Präparat, duale TAH)
- Sekundäre Endpunkte wurden vorher festgelegt
- CRUSADE-Score (Risiko schwerer Blutung post-MI) war in beiden Armen gleich hoch (42.39 vs 42.34 = 10%)
Limitationen ergeben sich leider aus der Durchführung als “Chart Review”: so ist nicht nachzuvollziehen, warum PatientInnen parenterale Antikoagulation erhielten - oder eben nicht. Vielleicht bot das heparinisierte Kollektiv initital ein schwereres Erkrankungsbild, worauf die Behandelnden aggressiver therapierten, was einen ziemlichen Spielraum für Interpretationsfehler lässt (vor allem respektive des Endpunkts Mortalität). Weiterhin waren beide Arme betreffend ACS-Risiko und Mortalität entsprechend GRACE-Score nicht ausbalanciert (PAK 132,14 vs nPAK 123,97). Viele PatientInnen wiesen sowieso ein niedriges oder moderates Risikoprofil auf, sodass ein vorteilshafter Effekt parenteraler Antikoagulation eventuell nicht deutlich gemacht wurde. Um einen substantiellen Anstieg des Mortalitätsrisikos bei nPAK auszuschließen fehlt es der Studie durch die generell niedrige Rate an Ereignissen (nur Erstereignisse wurden indexiert, keine Folgeereignisse) an Power.
#dasFOAM-Kommentar:
Parenterale Antikoagulation erscheint bei PatientInnen mit NSTEMI nicht mortalitätssenkend, erhöht aber im Vergleich zu rein peri-interventioneller Applikation das Risiko jeglicher Blutungsereignisse. Unter den limitierten Bedingungen der Studie lässt sich eine Hypothese formulieren, es werden jedoch dringend klärende RCTs benötigt.
Unfraktioniertes Heparin wird fast immer undifferenziert im ACS-Therapiebundle ohne Abwägung des Risiko-Nutzen-Verhältnisses und ohne vorherige Aufklärung des Patienten über etwaige Risiken verabreicht. Mit der vorliegenden Evidenz sollten wir eine routinemäßige Applikation bei NSTEMI und instabiler Angina Pectoris kritisch diskutieren, und dabei auch die empfangenden Schnittstellen wie Herzkatheterlabore und CPUs miteinbeziehen.
Wie immer gilt: Der Einzelfall entscheidet. Der Artikel erhebt keinen Anspruch auf Vollständigkeit oder Richtigkeit und die genannten Empfehlungen sind ohne Gewähr. Die Verantwortung liegt bei den Behandelnden. Der Text stellt die Position des Autors dar und nicht unbedingt die etablierte Meinung und/oder Meinung von dasFOAM.
Literatur:
- Chen, JY et al. Association of Parenteral Anticoagulation Therapy With Outcomes in Chinese Patients Undergoing Percutaneous Coronary Intervention for Non-ST-Segment Elevation Acute Coronary Syndrome. JAMA Intern Med 2018. PMID: 30592483
- Amsterdam EA et al. 2014 AHA/ACC Guideline for the Management of Patients with Non-ST-Elevation Acute Coronary Syndromes: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. JACC 2014. PMID: 25260718
- Nikolaou, N., Arntz, H., Bellou, A., Beygui, F., Bossaert, L., Cariou, A. and Danchin, N. (2015). European Resuscitation Council Guidelines for Resuscitation 2015 Section 8. Initial management of acute coronary syndromes. Resuscitation, 95, pp.264-277.
- https://rebelem.com/no-more-heparin-for-nstemi/
- Beitragsbild: https://www.pdchealthcare.com/en-001/


