Während des Lesens von Felix Beitrag über den Stellenwert von NaCl 0,9% im Rahmen des Therapieregimes von Patienten mit einer diabetischen Ketoazidose, ist mir ein schon etwas länger zurückliegender Artikel von Josh Farkas von PulmCrit eingefallen, den ich euch gerne als Ergänzung zu erwähntem Post hier nicht vorenthalten möchte. Wie immer als transkribierte Übersetzung und natürlich mit freundlicher Genehmigung des Autors.
Das Behandlungsregime der Azidose bei einer DKA sorgt häufig für Verwirrung. Es gibt nicht viel qualitativ gute Evidenz hierzu und wird es wahrscheinlich auch niemals geben . Dennoch kann uns ein grundlegendes Verständnis der physiologischen Grundlagen der DKA dabei helfen, diese rational und effektiv zu behandeln.
Physiologie der Ketoazidose bei einer DKA
Die Ketoazidose entsteht bedingt durch ein Ungleichgewicht zwischen verfügbarem Insulin und eigentlichem Insulinbedarf:
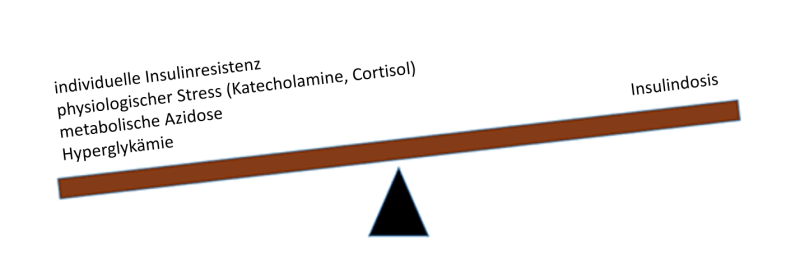
Es gibt mehrere Faktoren, die den Insulinbedarf beeinflussen:
- Patienten unterscheiden sich bereits ganz allgemein in ihrer grundsätzlichen Insulinresistenz und ihrem Insulinbedarf.
- Physiologischer Stress (z.B. durch Hypovolämie, Entzündungen) führen zu einem Anstieg der Katecholamine und von Cortisol, was wiederum die Insulinresistenz verstärkt.
- Hyperglykämie und metabolische Azidose an sich führen bereits zu einer erhöhten Insulinresistenz .
Die Behandlung einer DKA verläuft in der Regel in zwei Phasen: Zunächst gilt es mit der Ketoazidose fertig zu werden. Später müssen wir den Patienten dabei begleiten wieder zu seinem normalen Insulinspritzenschema zurückkehren zu können. Der Erfolg in beiden Phasen hängt davon ab den Insulinbedarf und die Insulindosis gut auszubalancieren.
Phase I (der Start): DKA mit heftiger Azidose - initiales Herangehen

Stellen wir uns einmal einen Patienten mit einer schweren DKA und einer besorgniserregenden Azidose vor. Das ist nicht allzu häufig. Punkte, welche Anlass zur Sorge geben, sind unter anderem folgende:
- Bikarbonat < 7 mmol/l
- pH < 7 (wenn er gemessen wurde; im Allgemeinen bringt es nur wenig Vorteil den pH überhaupt zu messen)
- klinisch schlechter Patient (z.B. Dyspnoe, dtl. Kussmaul’sche Atmung)
Meist haben diese Patienten eine schwere Azidose mit respiratorischer Kompensation. Das lässt zwei spezifische Sorgen aufkommen:
- Wenn sich die metabolische Azidose verschlechtert, werden sie wahrscheinlich dekompensieren.
- Um den pH einigermaßen halten zu können, sind die Patienten abhängig von der respiratorischen Kompensation. Wenn sie sich erschöpfen und damit ihre Fähigkeit zu hyperventilieren verlieren, wird der pH weiter fallen. Es ist also von entscheidender Bedeutung die Azidose umzukehren, bevor es zu einer Ermüdung oder einem respiratorischen Versagen (z.B. durch Aspiration oder Lungenödem) kommt .
Um diese Patienten zu stabilisieren und zu verbessern existieren mehrere Möglichkeiten:
(1) Insulin in ausreichender Dosierung
Die Schlüsseltherapie zur Ketoazidose ist Insulin. Je kränker der Patient ist, desto mehr Insulin wird er benötigen (weil Azidose, Hyperglykämie und Stress die Insulinresistenz erhöhen). Für die kränksten DKA-Patienten, kann die übliche Insulininfusion mit 0,1 I.E./kg/h häufig nicht ausreichend sein.
Insulinbolus als Loading-Dose

Früher war ein Insulinbolus von 0,15 I.E./kg i.v. vor Start des Perfusors Standard. Diese Heran-gehensweise ist in letzter Zeit etwas in Ungnade gefallen, da dies nach vorhandener Datenlage als nicht notwendig erscheint. Untersuchungen an Erwachsenen konnten weder einen signifikanten Nutzen noch einen Schaden durch die Anwendung eines Insulinbolus zeigen .
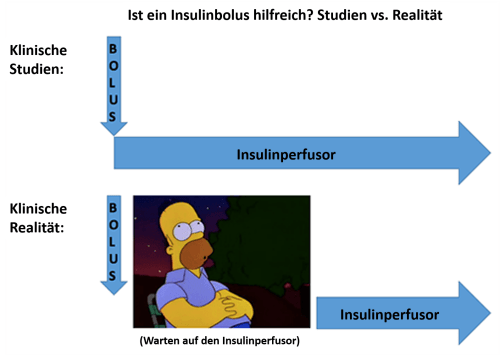
Nach dem Start einer Insulininfusion kommt es generell zu einem schnellen Anstieg der Insulinspiegel (vgl. Abbildung aus Kitabchi et al 2008). Auf eine initiale Bolusgabe zu verzichten hat in den ersten 15 Minuten subtherapeutische Dosen zur Folge, was aber von nicht allzu großer Bedeutung zu sein scheint.
Nichtsdestotrotz gibt es einen anderen Weg, über den ein Insulinbolus hilfreich sein kann. Es braucht ~45 Minuten für die Krankenhausapotheke um einen Insulinperfusor zu mischen und ihn an die entsprechende Abteilung auszuliefern. Währenddessen haben die meisten Notaufnahmen und Intensivstationen Ampullen mit 10 Einheiten Insulin auf Lager, was natürlich dann auch sofort gegeben werden könnte (mir sind Actrapidampullen von 10ml mit 40 I.E./ml geläufig). Durch die sofortige Applikation des vorrätigen Insulins kann somit ca. 1 Stunde früher ein therapeutischer Insulinspiegel erreicht werden, als wenn man nur einen Perfusor über die Apotheke ordert. Kommentar: Die hier beschriebene Praxis einen Perfusor über die Apotheke zu bestellen kommt mir für unsere Lande ziemlich fremd vor, bzw. ist mir eine derartige Handlungsweise an meinen bisherigen Arbeitsstellen nicht untergekommen. Dementsprechend ist es bei uns sicher nicht so, dass man 45 Minuten auf einen Perfusor warten muss, allerdings braucht auch das Mischen und Richten vor Ort sicher eine gewisse Zeit, insbesondere in personalangespannten Situationen, so dass sicher auch hier durch eine sofortige Bolusgabe eine gewisse Zeit überbrückt werden kann.
Für die meisten Patienten in einer DKA spielt das alles keine nennenswerte Rolle. Dennoch ergibt es Sinn den kränksten Patienten Insulin so schnell wie möglich zu verabreichen. Obwohl die Effektivität eines Initialbolus durchaus zu diskutieren ist, wurde er über Jahre routinemäßig angewendet und scheint zumindest bei Erwachsenen sicher zu sein (in pädiatrischen Patienten kann es dadurch zu einem erhöhten Risiko eines Hirnödems kommen) .
Manchmal reicht das veranschlagte Insulin nicht aus
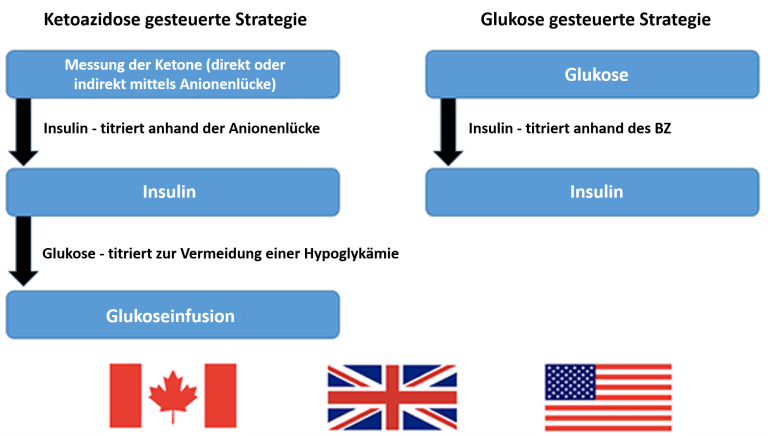
Die Anpassung der Insulindosis bei einer DKA kann entweder anhand der Ketoazidose oder anhand der Glukose gesteuert werden (vgl. Abbildung). So empfehlen z.B. die amerikanischen Leitlinien die Insulingabe anhand des Glukoselevels zu steuern (Kitabchi et al 2009), wohingegen die kanadischen Leitlinien empfehlen, sich am Ausmaß der Ketoazidose zu orientieren. Die britischen Leitlinien verwenden eine Mischung aus beiden, indem sie empfehlen sowohl die Ketone, als auch den Blutzuckerspiegel zu monitoren . Kommentar: Verfolgt man die deutschen Leitlinien der Erwachsenen und der Kinder zum Typ 1 Diabetes und der Ketoazidose wird auffällig, dass sich diese an allen anderen u.a. auch den australischen Leitlinien orientieren und somit auch eine Mischung aus allem vorhanden ist.
Beide Herangehensweise funktionieren in der Regel. Dennoch kann es Momente geben, in denen ein glukosebasiertes Protokoll nicht genug Insulin veranschlagt, um die Ketoazidose adäquat unter Kontrolle zu bringen. Die Gründe hierfür sind unter anderem:
- Hin und wieder haben Patienten eine schwere Ketoazidose ohne großartige Hyperglykämie. Das extremste Beispiel hierfür ist die euglykämische DKA, also eine Ketoazidose trotz normalem Blutglukosespiegel (z.B. durch Schwangerschaft, Hungern oder Gliflozine) .
- Die Serumglukose kann initial sinken allein durch einen Verdünnungseffekt im Rahmen einer Volumentherapie. Glukosebasierte Protokolle könnten Anlass geben, diesen Abfall als Hinweis dafür zu sehen, dass die Insulindosis bereits ausreicht (auch wenn sie es gar nicht tut).
Wenn eure Abteilung ein glukosebasiertes Protokoll verwendet, ist es wichtig sich dieser Stolpersteine bewusst zu sein. In manchen Fällen kann es notwendig sein vom vorgegebenen Protokoll abzuweichen und höhere Insulindosen zu applizieren (ggf. mit der zusätzlichen Substitution von Glukose um eine Hypoglykämie zu vermeiden) . Dies sollte immer in Betracht gezogen werden, wenn eine Ketoazidose nicht auf die Therapie des angewendeten Protokolls anspricht.
(2) Vermeide isotone Kochsalzlösung
Patienten mit einer DKA haben oft einen ziemlichen Volumenmangel. Diesen mittels Volumentherapie zu behandeln hilft gleichzeitig indirekt die Azidose zu beseitigen, indem es den physiologischen Stress reduziert (was wiederum zu einer Abnahme des Katecholamin- und Cortisolspiegels führt, mit daraus folgender verbesserter Insulinsensitivität).
Die meisten Leitlinien empfehlen hierfür isotone Kochsalzlösung zu verwenden (vgl. US, Kanada, GB, Dtl.-Erwachsene), aber hierbei handelt es sich immer noch um eine azidotische Flüssigkeit, welche die Azidose des Patienten verschlechtern wird. Eine balancierte, kristalloide Lösung, wie z.B. Ringer-Laktat, ist hier zu bevorzugen (vgl. auch einen älteren Post von Josh). Bei den meisten Patienten spielt dieser Unterschied sicher keine große Rolle, aber im Falle einer schweren Azidose ist es wahrscheinlich schon relevant. Kommentar: Wie eingangs bereits erwähnt sie hier nochmals auf den Beitrag von felixlorang verwiesen, der die Begründung der deutschen, respektive der britischen Leitlinie, warum NaCl 0,9% in deren Augen zu bevorzugen sei, unmissverständlich aufgearbeitet hat.
(3) Erwäge eine High-flow Nasenbrille
Sollte man sich darüber Sorgen machen, dass der Patient durch seine Kussmaul’sche Atmung eine respiratorische Erschöpfung erleidet, wäre eine Nasenbrille mit high-flow O2 (HFNC) eine sinnvolle Erwägung. Kommentar: für Hinweise bgzl. einer besseren Übersetzung von “high-flow nasal cannula” bin ich jederzeit dankbar. Hierbei handelt es sich nicht um die klassische 0815-Nasenbrille, welche uns allen geläufig ist. Vielmehr ist damit ein spezielles System gemeint, welches erlaubt Sauerstoff via besonderer Nasenbrille, erwärmt und angefeuchtet mit relativ hohen Flussraten zu applizieren und als Alternative zur NIV dienen kann. Zu weiterführenden Informationen diesbezüglich: LITFL, Resus.me, REBELEM, Scancrit. Das Ziel ist es, die Flussrate zur Hilfe zu nehmen, um das CO2 weiter zu senken (durch Reduzierung des anatomischen Totraumes und Verbesserung der Effizienz der Ventilation).
Hierzu existiert keine wirkliche Literatur. Evidenz, die dies unterstützt, wären unter anderem:
 Es konnte gezeigt werden, dass HFNC in der Lage ist die Atemfrequenz und Atemarbeit in anderen Zusammenhängen zu senken.
Es konnte gezeigt werden, dass HFNC in der Lage ist die Atemfrequenz und Atemarbeit in anderen Zusammenhängen zu senken. - In der Regel schaffen es DKA-Patienten nicht ihren PaCO2 unter ~10mmHg zu bringen. Mittels HFNC können überraschend niedrige PaCO2-Werte gesehen werden, was die Annahme unterstützt, dass HFNC die CO2-Beseitigung unterstützt.
In der Regel wird dies in den meisten Fällen nicht notwendig sein, aber es kann helfen und ist sicher in der Anwendung. Im Gegensatz dazu gibt es bei der BiPAP ein gewisses Aspirationsrisiko, insbesondere dadurch, dass diese Patienten einen Hang zur Gastroparese und Erbrechen haben.
(4) Bicarbonat lenkt nur ab.
Eine Frage, die in diesen Fällen immer wieder auftaucht: “Bikarbonat geben, oder nicht?” Ganz einfach gesagt handelt es sich hierbei schlicht um die falsche Frage. Eine bessere Frage wäre: “Wie kann ich am schnellsten die Ketoazidose des Patienten regulieren?” (Antwort: Viel Insulin, Flüssigkeit, Glukose, Kalium, Behandlung der zugrundeliegenden Ursache.)
Diese Patienten brauchen kein Bikarbonat - was sie brauchen ist ein maximal aggressives Management ihrer DKA. Es gibt keine Evidenz, dass Bikarbonat bei der Behandlung einer Ketoazidose funktioniert. Vielmehr fungiert Bikarbonat hier eher im Sinne einer gefährlichen Ablenkung und lässt uns die eigentlich dringender notwendigen Behandlungen aus den Augen verlieren.
Phase II (die Landung): Weiterführende Be handlung der Azidose bis zum Abschalten des Insulinperfusors

Betrachten wir nun ein viel häufigeres Problem: Patienten, bei denen sich die Anionenlücke ausgeglichen hat, die aber weiterhin eine metabolische Azidose haben, diesmal ohne Anionenlücke (bzw. mit normaler Anionenlücke; wer nochmal einen kurzen Überblick zur Anionenlücke im Allgemeinen braucht, sei hiermit auf Wiki verwiesen. Im weiteren Verlauf wird der Begriff “ohne Anionenlücke” mit “normaler Anionenlücke” gleichgesetzt, da es unter normalen Umständen physiologisch immer eine leichte Lücke gibt. Ich bitte diese Ungenauigkeit zu entschuldigen). Häufig bleiben Patienten nach Ausgleich der Ketoazidose bei einem Bikarbonat um die 12-18 mmol/l. Eine Azidose ohne Anionenlücke tritt meist aufgrund folgender beider Punkte auf:
- Volumentherapie mit isotoner Kochsalzlösung oder 0,45% NaCl.
- Ausscheidung von Ketosäuren über den Urin mit Verlust von “potentiellem Bikarbonat”.
Warum sollte uns das kümmern?
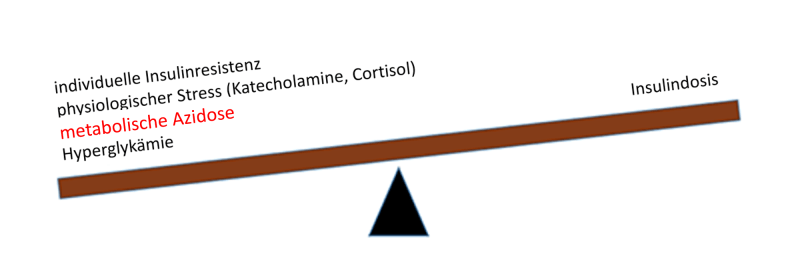
Die klinische Bedeutung einer Azidose ohne Anionenlücke ist im allgemeinen schon diskutierbar. Bei einer DKA ist sie allerdings aus zwei Gründen problematisch:
- Die meisten Behandlungsprotokolle verlangen, dass ein Bikarbonat von >15mmol/l erreicht sein muss, bevor man den Insulinperfusor stoppen darf.
- Eine metabolische Azidose erhöht die sog. Insulinresistenz. Meiner Meinung nach kann bereits eine leichte Azidose (z.B. Bikarbonat 15-20mmol/l) das Risiko erhöhen eine erneute DKA zu bekommen, nachdem das Insulin gestoppt wurde:
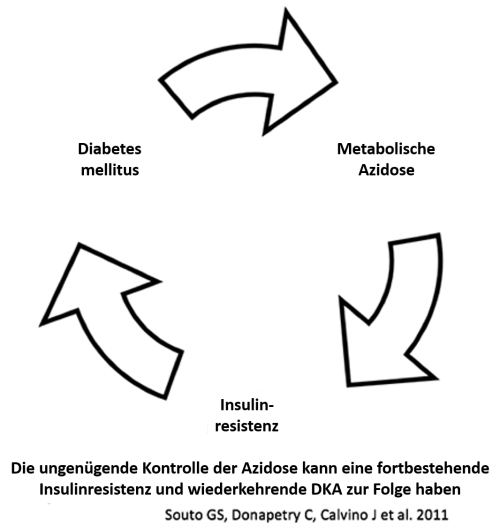
Bikarbonat - eine logische Therapie bei metabolischer Azidose ohne Anionenlücke
Wie oben bereits angesprochen handelt es sich bei Bikarbonat um eine irrationale Therapie bei einer Ketoazidose. Dem gegenüber steht Bikarbonat allerdings als durchaus logische Therapie für eine metabolische Azidose ohne Anionenlücke, da dies einen wesentlichen Mangel an Bikarbonat widerspiegelt . Ohne diese Therapie kann es eine Weile dauern bis die Nieren des Patienten in der Lage sind wieder genug Bikarbonat zu bilden und somit die Azidose ohne Anionenlücke zu korrigieren.
Grundzüge der Bikarbonattherapie
Am besten infundiert man isotones Bikarbonat zum Ende der DKA-Therapie . Wenn die Anionenlücke wieder annähernd geschlossen ist, kann der endgültige Bikarbonatspiegel abgeschätzt werden (unter der Annahme, dass die Anionenlücke bei ~10mM bleibt):
Berechneter endgültiger Bikarbonatspiegel = Bikarbonatspiegel + Ketonspiegel
Ketonspiegel = Anionenlücke - 10 = (Na - Cl - Bikarbonat) - 10
=> Berechneter endgültiger Bikarbonatspiegel = Na - Cl - 10
Wenn der berechnete endgültige Bikarbonatspiegel sehr niedrig ist, dann kann isotones Bikarbonat gegeben werden (1l Glukose 5% mit 150ml Bikarbonat (8,4%), generiert eine Lösung mit 150mmol Bikarbonat und 130mmol/l) . Das schlussendlich benötigte Volumen kann abgeschätzt werden, indem man das Bikarbonatdefizit berechnet (1 Liter ist in der Regel schon mal nicht ganz verkehrt).
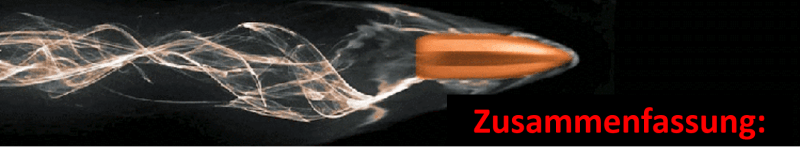
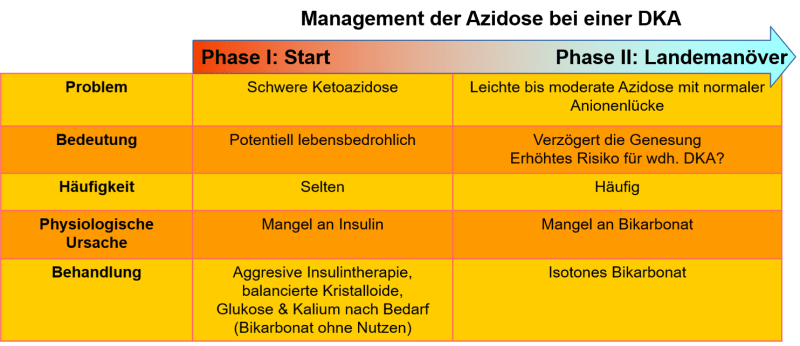
- Während der Therapie einer DKA können Patienten unterschiedliche Arten einer metabolischen Azidose präsentieren. Das physiologische Problem zu verstehen, kann ein logische und effektive Behandlung erleichtern.
- Mitunter gibt es Patienten mit einer wirklich schweren Ketoazidose. Die Behandlung derselben beinhaltet ein maximal aggressives Herangehen an die DKA:
- Adäquate Insulindosis (ggf. mit einem Initialbolus)
- Aggressive Volumentherapie mit balancierter Vollelektrolytlösung
- Ggf. der Gebrauch einer High-flow Nasenbrille (HFNC), um die respiratorische Kompensation durch den Patienten zu unterstützen
- Viele Patienten werden während der Besserungsphase eine leichte Azidose ohne Anionenlücke haben. Auch wenn es sich hierbei um keinen lebensbedrohlichen Zustand handelt, kann dies den Aufenthalt verlängern und das Risiko erhöhen in eine erneute DKA nach Beendigung des Insulinperfusors zu rutschen. Eine rationale Therapie für diese Problem ist isotone Bikarbonatlösung.
Weiterführende Posts:
- DKA pearls (PulmCrit)
- Bikarbonat bei DKA? Vgl. Chris Nickson von LITFL, Anand Swaminathan von EMDocs, Salim Rezai von RebelEM, Darrel Hughes von RebelEM.
- Insulinbolus? Darrel Hughes von RebelEM
- Euglykämische DKA: Craig Cocchio on RebelEM
- ABG/VBG ohne großen Benefit bei einer DKA (PulmCrit)
Fußnoten:
Eine randomisierte, kontrollierte Studie an Patienten mit einer DKA und schwerer Azidose (d.h. pH <6,9) durchzuführen wird aufgrund der Seltenheit und der Dringlichkeit der Behandlung nur sehr schwierig durchzuführen sein. Wahrscheinlich sind die logistischen Voraussetzungen bzgl. Rekruitment und Einwilligung für eine derartige Studie zumindest in den USA unüberwindbar.
Die meisten Patienten hyperventilieren selbst effektiver, als es an einer Beatmungsmaschine möglich wäre. Aufgrund dessen wird am besten versucht eine Intubation zu vermeiden, da sie das Problem nicht zwangsläufig lösen wird. Für weitere Informationen diesbezüglich vgl. Pearl #3.
Bitte beachtet, dass sich dieser Beitrag und eigentlich der gesamte PulmCrit-Blog nur auf Erwachsenenmedizin beschränkt.
Eine Ketoazidose kann entweder direkt (durch einen Point-of-care Ketonmesser oder vielleicht auch durch Messung des Beta-Hydroxybutyratspiegels) oder indirekt (über Ermittlung der Anionenlücke) gemessen werden. Die britischen Kollegen scheinen eher eine Point-of-care-Messung zu verwenden, wohingegen dies in den Vereinigten Staaten eher selten anzutreffen ist.
Bei “Glitoflozinen” handelt es sich um eine neuere Klasse oraler Medikamente für den Diabetes Typ-2, u.a. CANAglifozin (bei uns außer Handel), DAPAgliflozin, EMPAgliflozin (und ERTUgliflozin), die über eine Hemmung des Natrium-Glukose-Transportproteins 2 (SGLT-2, deswegen auch SGLT-2-Hemmer) ihre Wirkung entfalten und es dadurch zu einem Glukoseverlust über den Urin kommt. Es finden sich immer mehr Hinweise und es wird auch zunehmend anerkannt, dass diese Medikamente zu einer euglykämen DKA führen können. Mehr Informationen diesbezüglich finden sich hier.
In erster Linie im Rahmen eines Wechsel von einer Glukose gesteuerten Strategie hin zu einer Ketoazidose gesteuerten Strategie.
Oder einem Übermaß an Chlorid, wenn man es bevorzugt von diesem Standpunkt aus betrachten möchte (ganz im Sinne von P. Stewart)
Natürlich kann dies auch nach dem Ausgleich der Anionenlücke gemacht werden. Die frühzeitige Infusion von Bikarbonat kann diesen Prozess aber etwas beschleunigen.
Der Zucker wird durch die Zellen absorbiert, so dass er physiologisch gesehen nicht effektiv osmotisch wirksam wird. Der Grund Glukose 5% zu verwenden (anstatt von Wasser) liegt einfach darin begründet, dass die meisten Krankenhäuser kein steriles Wasser zur Infusion vorhalten. Würde man das Bikarbonat ohne vorherige Verdünnung in der Glukose geben, würde man eine Hypernatriämie provozieren, weil Bikarbonat ungefähr die gleiche Osmolarität wie 6% Natriumchlorid besitzt.



Sehr schöner Artikel. Vielen Dank dafür.
Im Artikel wurde die Kaliumgabe leider nur kurz erwähnt, ist aber extrem wichtig, da durch die adäquate Behandlung der DKA der Kaliumspiegel schnell massiv fallen kann (d.h. frühzeitige Kaliumgabe)
weiterführende Literatur: IBCC Kapitel DKA:
http://emcrit.org/ibcc/dka/
Zum isotonen NaBi: 1000ml G5 und 150 ml 8,4% NaBi ist super, leider aber praktisch schwierig umzusetzen, da es in Deutschland nur 100ml und 250ml Flaschen gibt (lt. Roter Liste auch 20ml von Köhler Pharma). Ich hab die Erfahrung gemacht, dass 500ml G5 und 100ml NaBi eigentlich eine gute Alternative sind. Die 100ml passen genau in die 500ml-Flasche (G5 von Bernburg). Das würde eine leicht hypertone Lösung generieren (~ 333 mosmol/l) ist aber praktisch und wirtschaftlich meiner Meinung nach sinnvoller.
(es bestehen keine Interessenkonflikte 😜)
Kleiner Funfact: G5 hat ja eine Osmolarität von ca. 280mosmol/l und wenn wir jetzt NaBi dazugeben (bei 150ml in 1000ml G5) erhalten wir eine Osmolalität von ca. 500 mosmol/l, da jedoch die Glukose schnell metabolisiert wird, kann man die Osmolarität der G5 „vernachlässigen“.
Hallo Thomas,
vielen Dank für deine Anmerkungen. Hinsichtlich des Kaliums kann ich dir natürlich nur zustimmen. Das Hauptziel dieses Beitrags war allerdings auf das Management der Azidose einzugehen. Hinsichtlich der kompletten Therapie einer DKA gehen wir sicherlich in Zukunft nochmal etwas genauer ein (zur Komplettierung sozusagen). Danke auch für dein eigenes Kochrezept zur Herstellung einer nahezu isotonen Bikarbonatlösung.